在体全细胞膜片钳研究综述
本文改编自: In Vivo Whole-Cell Patch-Clamp Methods: Recent Technical Progress and Future Perspectives
大脑功能是生物体生存的基础,它们由各种神经元组成的神经回路支持。为了在单细胞水平上研究神经元的功能,研究人员经常使用全细胞膜片钳记录技术。这些技术使我们能够记录动物的单个神经元的膜电位(包括动作电位)。这种全细胞记录方法使我们能够揭示神经元活动如何在单细胞水平上支持大脑功能。本文,我们将介绍以前使用在体膜片钳记录技术的研究,以及主要关于海马中神经元活动对行为功能的最新发现。我们进一步讨论了如何拉近电生理学和生物化学之间的距离。
1. 简介
神经元网络的动作电位是十分精妙绝伦的,每个动作电位都由突触输入的时空总和触发,这是大脑功能的基本组成。为了研究神经活动,研究人员开发了各种类型的电生理记录技术,大致分为细胞外和细胞内方法。虽然细胞外记录使我们能够获得有关记录电极周围多个细胞产生的神经元放电和集体振荡动力学的数据,但细胞内记录允许测量单细胞水平的阈下膜电位动态和阈上放电活动(图 1a)。根据记录电极尖端的厚度,这些细胞内记录进一步分为膜片钳和尖锐电极技术。不过,尖锐电极的较高阻抗会导致较大的漏电流并妨碍电压钳记录。膜片钳法是唯一能够以高信噪比捕获单个神经元细胞内活动的方法。
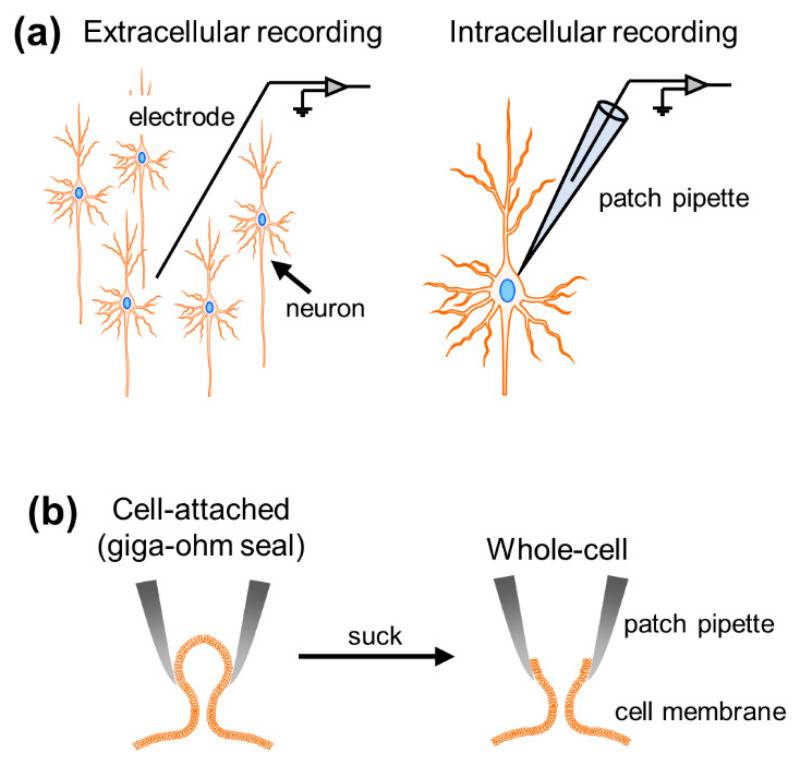
研究员对神经元进行膜片钳实验,首先需要拉制玻璃电极(玻璃电极一般直径约为 3µm,电阻为 3-7MΩ)。然后,他们用人工细胞内液填充玻璃电极,并将电极与记录装置中的电极夹持器连接,玻璃电极中会插入有 AgCl 涂层的导线,导线会接触电极内液。完成准备后,他们将玻璃电极压在细胞膜上,并在吸管和膜之间以 >1 GΩ 的电阻将膜紧紧封接在一起,称为千兆欧姆封接。这种模式也称为“单通道模式”(图 1b)。这种记录模式使我们能够捕捉离子通过细胞膜上的离子通道产生的膜电流的动态。溯源来看,膜片钳法最初就是为了记录单通道电流而开发的。一旦施加负压并在细胞膜上形成一个小孔(全细胞模式),就可以测量通过细胞膜上表达的所有离子通道产生的全细胞电流和电压的净动态。通过将电压保持在特定值(电压钳)就可以记录反映神经元突触输入的全细胞电流,而通过控制钳制电流(电流钳)则可以记录动作电位,或者低于放电阈值的膜电位波动。尽管膜片钳方法中还有其他记录模式,但本文将重点关注电压钳和电流钳配置中的全细胞记录模式。
2. 麻醉动物的在体全细胞记录
2.1 大脑皮质
在体全细胞记录最早是在麻醉的动物身上开展实验的。这是因为建立稳定的 GΩ 封接是全细胞记录的关键过程,想要达到高信噪比,要求大脑尽可能静止。早期阶段的靶向区域是主要的视觉皮质(V1)和初级躯体感觉皮质(S1),因为这些皮质靠近大脑外面,比其他大脑皮质区域更容易进入。研究人员钳制神经元时,对神经元形态和电极位置,没有实际视野,这种无视野控制电极的方法,被称为“盲插”。
在 1994 年,有研究使用全细胞记录用于研究 GABA 输入对猫 V1 椎体神经元的方向选择性的影响,膜片钳用于记录超阈值和亚阈值活动1(图 2a)。该研究表明,尽管在细胞内使用 GABA 受体阻断剂阻断了亚阈值电活动,但 V1 神经元仍然以方向选择的方式激发了动作电位,表明兴奋性输入足以产生方向选择性。
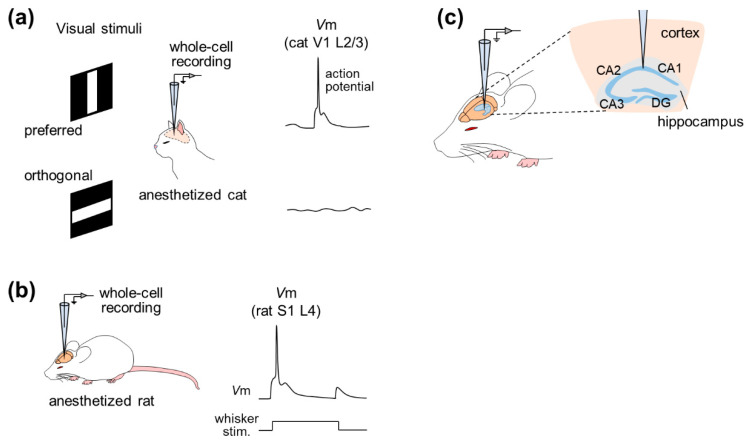
随后,全细胞记录方法被广泛应用,特别是大鼠桶状皮层,他是 S1 的一个子区域,其活动与胡须触觉行为相关。通过戊巴比妥麻醉下的全细胞记录对胡须(特殊的触觉胡须)刺激的内在特性和亚阈值反应可以进行研究2。然后,一系列研究通过聚氨酯麻醉下大鼠桶状皮层的记录和记录细胞的事后重建精确描述了晶须偏转的动态感受野3,4,5(图 2b)。除了进行事后可视化或重建之外,膜片钳记录还可以与氨基甲酸乙酯麻醉大鼠的皮质神经元的基因操作和光学成像相结合6。有研究使用慢病毒载体进行神经元特异性基因传递,使用基于双光子显微镜的技术分析单个皮层细胞水平的表型。这项研究使用高分辨率双光子延时成像来监测树突棘和轴突的结构,并通过双光子显微镜引导的全细胞记录同时测量电生理学上的细胞反应。这种方法非常适用于将电生理功能与完整大脑中单个神经元中的基因表达相关联,但是该方法在清醒动物中的可行性还未得到证实。
2.2 海马等区域
除了对大脑新皮层的研究之外,麻醉动物的全细胞记录也研究了其他区域,例如研究大脑中的嗅皮层、海马体、基底外侧杏仁核、梨状皮质和丘脑等。另外甚至也有研究脑干和小脑的。
Hahn等人,首次实现了对内嗅锥体细胞、海马锥体细胞、齿状颗粒细胞甚至海马中间神经元的在体全细胞记录 7,8,9(图 2c)。氨基甲酸乙酯麻醉下通过同时记录 CA1 锥体细胞、CA3 锥体细胞和齿状颗粒细胞的新皮质局部场电位 (LFP) 和膜电位显示,这三种类型的细胞受到皮质网络振荡的调节,表明新皮质之间的各种功能连接和海马各个亚区。此外,位于辐射层和腔隙层-分子边界的海马中间神经元的膜电位与新皮质的状态几乎完全同步,延迟很小,表明新皮质活动驱动海马中间神经元的膜电位波动。最近,双电极全细胞记录已被用于研究海马神经元之间的关系10。
基底外侧杏仁核 (BLA) 中神经元的全细胞记录,在体内位于比海马体更深的位置。研究表明,BLA 神经元表现出以大约 0.3 Hz 的频率出现的缓慢振荡。在波动状态期间使用体感刺激(即足部电击)、听觉刺激或丘脑后部刺激,研究表明 BLA 中的振荡活动是由皮层神经元的集合驱动的,并且这些集合以状态依赖的方式控制杏仁核神经元对厌恶刺激的反应;也就是说,厌恶刺激在神经网络处于波谷状态时有效,但在神经网络处于波峰状态时无效11,12,13。
Brecht 和 Sakmann 在 2002 年实现了丘脑神经元的在体全细胞记录。由于丘脑的腹后内侧核 (VPM) 是桶状皮层胡须(晶须)驱动输入的主要来源,因此他们针对这一大脑区域进行研究,并描述了两类主要的 VPM 神经元:单晶须激发细胞和多晶须激发细胞。前者表现出对特定单个晶须刺激的亚阈值或超阈值反应,而后者表现出对多个晶须刺激的反应。此外,他们证明这两种细胞类型在感受野的大小、对晶须偏转的响应模式、抑制输入的强度和内在特性方面是不同的14。
Häusser 小组的一系列研究探索了小脑中的信息处理。小脑是一个有利的模型系统,用于解决感觉诱发的突触输入和由此产生的输出尖峰模式之间的关系,因为小脑中的颗粒细胞构成输入层,将苔藓纤维信号转化为平行纤维输入到浦肯野细胞。例如,石川等人。解决了小脑皮质输入阶段的单个小脑颗粒细胞如何整合多感觉(即体感、听觉和视觉)信号的问题。使用全细胞电压钳记录,他们描述了神经元对感觉、听觉、视觉刺激或这些刺激的收敛作出反应,并表明多感觉输入的组合可以增强颗粒细胞的尖峰输出15,16,17,18,19。
盲插法膜片钳很难具体定位记录的细胞,研究人员开发了“靶向膜片钳”技术来记录新皮质中特定靶细胞的膜电位。该方法有“双光子靶向膜片钳”和“细胞阴影膜片钳”两种方式。
Margrie 等人。首先将双光子成像结合到在体膜片钳方法中,并开发了体内靶向钳技术,以将玻璃电极引导至体内单个被标记的皮层神经元(“双光子靶向钳”,图 3a)。 Margrie 等人使用转基因小鼠,其小白蛋白阳性中间神经元被标记有增强的绿色荧光蛋白 (eGFP)。在 S1 中对小白蛋白阳性中间神经元进行膜片钳记录。他们描述了中间神经元的内在特性,从而揭示了 S1 神经元的自发和感觉诱发活动模式20。此外,Kitamura 等人。建立了阴影膜片钳方法,其中使用膜片钳电极用荧光染料灌注目标神经元的细胞外空间,使神经元可视化为负图像(“阴影”)并根据其体细胞和树突结构进行识别。然后,他们在视觉控制下将相同的电极放置在神经元上,以从大鼠和小鼠的新皮质和小脑中视觉识别的神经元获得膜片钳记录(“阴影膜片钳”;图 3b)。他们还利用质粒 DNA 的靶向体内单细胞电穿孔进入已识别的细胞类型,从而实现稳定的转基因表达21。这些技术不仅加速了电生理记录,还加速了完整幼稚动物单个神经元的标记和基因操作。
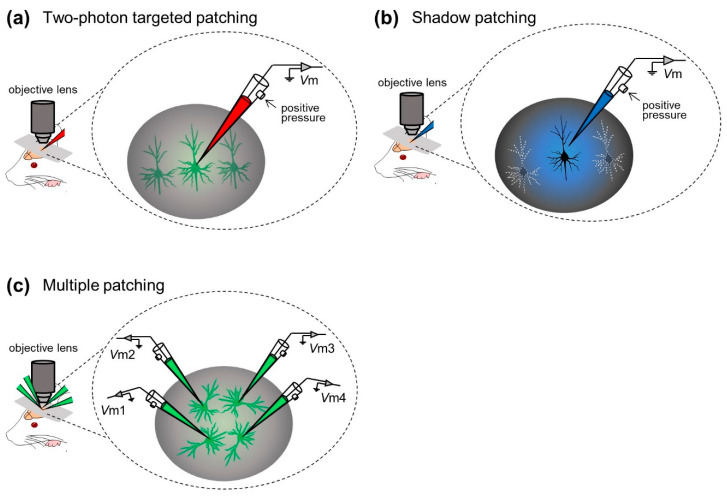
在上述大多数研究中,研究人员在试验中捕获了单个神经元的膜电位动态。尤其是在“盲插”条件下,即使是单个全细胞记录也只能在概率上实现。一般来说,多个神经元的同时全细胞记录在技术上具有挑战性,因为多个玻璃电极的运动会相互干扰并破坏稳定的封接。然而,Jouhanneau 等人。通过同时从多达四个新皮质神经元进行靶向膜片钳记录来解决这个问题(图 3c)。他们描述了阈下水平的细胞之间信息处理的相似性或差异,并揭示了皮质神经元之间的突触连接22,23,24,25。
3. 清醒状态下动物在体全细胞记录
3.1 大脑新皮质
Margrie 等人,在对大鼠进行手术和膜片钳记录之前几天,就开始训练老鼠在记录装置中保持静止。这种训练是费力但很重要的,因为不习惯的动物会不停的挣扎或试图逃离记录装置。作者首先报道了清醒状态下啮齿动物桶状皮质的全细胞记录,并观察到了响应晶须刺激的膜电位去极化26。随后,Poulet 等人。和 Yu 等人。证明了在自主胡须行为期间小鼠胡须桶皮层的去同步状态是由丘脑的放电活动增加触发的,并且与部分中间神经元的活动相关27,28。
此后各种研究报告了有意识状态下的啮齿动物和猴子对外部刺激的阈下反应。此外,研究人员将在体全细胞记录应用于清醒啮齿动物的其他皮层区域,包括初级运动皮层 (M1)、前外侧运动皮层 (ALM)、前额叶皮层和初级听觉皮层 (A1)。值得注意的是,Bitzenhofer 等人,成功地对发育中的新生大鼠进行全细胞记录29。此外,Guo 等人和 Inagaki 等人。揭示了执行学习任务的清醒小鼠 ALM 中持续神经活动的膜电位动力学30,31。最近,还有报告研究了清醒状态下啮齿动物社交接触的阈下膜电位相关性32,33,34。
3.2 海马等区域
与新皮质相比,大脑边缘系统位于大脑内部和更深处。关于使用电极从体内深层区域进行侵入性记录,从预期区域本身进行记录的可能性很低,因为大脑中电极的准确位置对实验者是无法预知的。此外,为了成功进行全细胞记录,玻璃电极的电极尖端必须尽可能保持清洁,以在细胞膜上形成高电阻密封。当研究人员试图记录体内深层区域的膜电位时,一些“障碍物”,如细胞外基质和血管很有可能粘附在电极尖端上。肮脏的尖端妨碍千兆欧姆的封接,导致从麻醉和清醒动物的深层区域进行全细胞记录的成功率很低。因此,从活体动物的深层区域进行全细胞记录在技术上很难实现,但一些研究人员试图解决这个问题。解决方案之一是通过吸力去除新皮质。本文回顾了以前对技术问题提出挑战的研究,并为动物行为学的神经相关性提供了新的见解。
我们专注于海马体和内侧内嗅皮层,这两者对于外部环境的表征都是必不可少的。与外部环境最有名的海马神经相关物是位置细胞,当动物穿过环境中的特定位置(称为“位置场”)时,它们会选择性地激发动作电位。虽然这种特定于位置的放电率增加被称为位置细胞的“速率代码”,但它们相对于正在进行的海马 θ 振荡相位的精确尖峰时间在动物接近位置场(即“θ 相位岁差”),称为“时间码”。这些超阈值活动通过细胞外记录进行了描述,但位置代码的细胞内动力学仍然难以捉摸。
为了检查双码的机制,Harvey 等人。首先使用在体全细胞记录方法监测在虚拟现实环境中导航的小鼠位置细胞的细胞内动态35(图 4a)。当动物沿着虚拟线性轨道来回奔跑时,他们获得了海马神经元强大的位置选择性放电活动,并确定了位置场的三个亚阈值特征:(1)基线膜电位的不对称斜坡状去极化,(2)细胞内θ振荡幅度的增加,和(3)细胞内θ振荡相对于细胞外记录的 θ 节律的相位进动。这些结果表征了位置细胞的速率和时间代码背后的细胞内动力学。 Harvey 等人介绍的虚拟现实系统。为研究空间导航神经回路的新实验方法打开了大门。
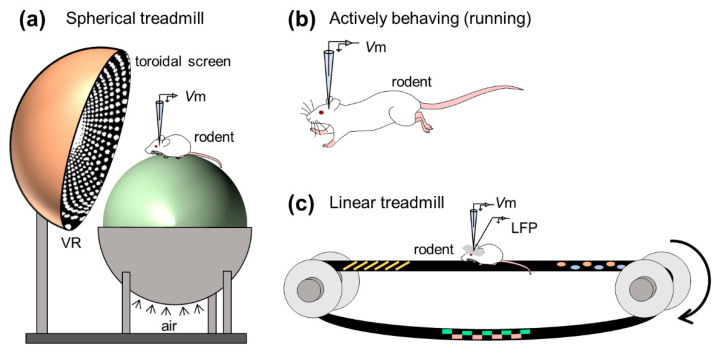
对能够自由移动的啮齿动物的进行全细胞记录在技术上更具挑战性(图 4b)。这是因为啮齿动物在记录过程中的突然的行为会导致大脑的较大幅度运动,这会导致电极封接不稳定。高电阻封接甚至对大脑的细微运动也很敏感,因为电极尖端的直径约为 3 μm,而大鼠和小鼠的锥体神经元的胞体长度约为 20 μm。尽管存在技术困难,Lee 等人还是成功对自主行为动物进行全细胞记录36。随后 Epsztein 等人报道了幅度小于峰值电位的膜电位的快速事件,称为峰值前电位37。他们随后检查了大鼠在环境中自由导航时海马 CA1 亚区中位置细胞和静默细胞(即在环境探索过程中不发出尖峰放电的细胞)之间的内在差异,发现与静默细胞相比,位置细胞的尖峰阈值较低。探索的开始和未来的定位细胞在探索之前可能会表现出更高的突发放电38。在另一项研究中,Lee 等人。进一步尝试通过玻璃电极注入正电流来人为地诱导海马细胞空间均匀去极化,并发现即使在沉默细胞中也会突然和可逆地出现空间调谐的亚阈值响应和位置特异性放电39。因此,他们解释突触后神经元兴奋性门控突触前输入,并提出了一种独特的细胞机制来生成位置代码。在这些研究之后,啮齿动物边缘系统空间表征的细胞内机制,包括海马体和内侧内嗅皮层都被广泛的研究了。
海马体产生细胞外电振荡,反映了神经阈上放电和阈下突触活动的集合,并在学习、记忆和空间导航中发挥重要作用。特征性细胞外振荡(通常称为 LFP),特别是在海马中,是(1)θ 振荡(3-10 Hz)和(2)尖波-波纹复合物(SWR),由尖波(2-30 Hz)组成)和瞬态纹波振荡(100-250 Hz),它们分别有助于(1)记忆编码和(2)记忆巩固。为了寻找与学习和记忆相关的膜电位,研究人员经常捕获清醒啮齿动物海马的阈下动力学和场振荡,特别关注 SWR,了解海马神经元在其他细胞外振荡频带期间的细胞内特征(图 4c)。
English D.F.等人首次使用尖锐电极在 SWR 期间实现细胞内记录40。他们成功地从自由奔跑的动物身上进行记录,并在 SWR 期间发现 CA1 锥体细胞中一致的大去极化,这与称为细胞内波纹的膜电位的瞬态波纹频率波动有关。请注意,在相邻区域(即海马下托)也观察到细胞内波纹41。随后的一系列研究精确地描述了亚阈值活动以及海马 SWR。 Hulse 等人。对在跑步机上奔跑的动物进行全细胞记录,发现海马波纹事件周围的膜电位包括(1)与尖波相关的去极化,(2)叠加在细胞外波纹上的细胞内高频波纹状振荡,以及(3)波纹后的超极化。他们进一步指出,在 SWR 期间,单个海马锥体细胞的精确激活需要激发和抑制之间的平衡 42。这些对与 SWR 相关的细胞内动力学的研究表明,在细胞外波纹事件期间,峰值放电输出背后的突触机制,这将有助于记忆巩固。
与其对记忆的贡献一致,海马体相关的疾病就是阿尔茨海默病和癫痫。例如,Šišková 等人。对阿尔茨海默病小鼠模型的海马锥体神经元进行体内全细胞记录,同时进行高分辨率受激发射耗尽显微镜成像和计算建模。他们证明,突触输入到动作电位输出的分支结构依赖性放大将代表网络功能障碍的细胞病理机制,并表明这种病理机制可能与其他具有异常树突形态的神经退行性疾病有关43。
到目前为止,我们介绍了以前的研究,调查了突触输出背后的突触机制,特别是集中在新皮质、海马和海马邻近区域。清醒哺乳动物的体内全细胞记录已在各个领域进一步实现,包括嗅球、丘脑、小脑、侧隔和蝙蝠的下丘。请注意,这些对下丘的体内全细胞记录研究是在清醒的蝙蝠中进行的,因为蝙蝠的下丘没有被新皮质或小脑覆盖,并且可以通过颅骨视下看到。
未完待续
参考文献
- Nelson S., Toth L., Sheth B., Sur M. Orientation selectivity of cortical neurons during intracellular blockade of inhibition. Science. 1994;265:774–777.
- Zhu J.J., Connors B.W. Intrinsic Firing Patterns and Whisker-Evoked Synaptic Responses of Neurons in the Rat Barrel Cortex. J. Neurophysiol. 1999;81:1171–1183.
- Brecht M., Roth A., Sakmann B. Dynamic Receptive Fields of Reconstructed Pyramidal Cells in Layers 3 and 2 of Rat Somatosensory Barrel Cortex. J. Physiol. 2003;553:243–265.
- Manns I.D., Sakmann B., Brecht M. Sub- and suprathreshold receptive field properties of pyramidal neurones in layers 5A and 5B of rat somatosensory barrel cortex. J. Physiol. 2004;556:601–622.
- Brecht M., Sakmann B. Dynamic representation of whisker deflection by synaptic potentials in spiny stellate and pyramidal cells in the barrels and septa of layer 4 rat somatosensory cortex. J. Physiol. 2002;543:49–70.
- Dittgen T., Nimmerjahn A., Komai S., Licznerski P., Waters J., Margrie T.W., Helmchen F., Denk W., Brecht M., Osten P. Lentivirus-based genetic manipulations of cortical neurons and their optical and electrophysiological monitoring in vivo. Proc. Natl. Acad. Sci. USA. 2004;101:18206–18211.
- Hahn T.T.G., McFarland J.M., Berberich S., Sakmann B., Mehta M.R. Spontaneous persistent activity in entorhinal cortex modulates cortico-hippocampal interaction in vivo. Nat. Neurosci. 2012;15:1531–1538. doi: 10.1038/nn.3236.
- Hahn T.T.G., Sakmann B., Mehta M.R. Differential responses of hippocampal subfields to cortical up-down states. Proc. Natl. Acad. Sci. USA. 2007;104:5169–5174. doi: 10.1073/pnas.0700222104.
- Hahn T.T.G., Sakmann B., Mehta M.R. Phase-locking of hippocampal interneurons’ membrane potential to neocortical up-down states. Nat. Neurosci. 2006;9:1359–1361. doi: 10.1038/nn1788.
- Liu Y.-Z., Wang Y., Shen W., Wang Z. Enhancement of synchronized activity between hippocampal CA1 neurons during initial storage of associative fear memory. J. Physiol. 2017;595:5327–5340. doi: 10.1113/JP274212.
- Windels F., Yan S., Stratton P.G., Sullivan R., Crane J.W., Sah P. Auditory Tones and Foot-Shock Recapitulate Spontaneous Sub-Threshold Activity in Basolateral Amygdala Principal Neurons and Interneurons. PLoS ONE. 2016;11:e0155192. doi: 10.1371/journal.pone.0155192.
- Windels F., Crane J.W., Sah P. Inhibition Dominates the Early Phase of Up-States in the Basolateral Amygdala. J. Neurophysiol. 2010;104:3433–3438. doi: 10.1152/jn.00531.2010.
- Crane J.W., Windels F., Sah P. Oscillations in the basolateral amygdala: Aversive stimulation is state dependent and resets the oscillatory phase. J. Neurophysiol. 2009;102:1379–1387. doi: 10.1152/jn.00438.2009.
- Brecht M., Sakmann B. Whisker maps of neuronal subclasses of the rat ventral posterior medial thalamus, identified by whole-cell voltage recording and morphological reconstruction. J. Physiol. 2002;538:495–515. doi: 10.1113/jphysiol.2001.012334.
- Chadderton P., Margrie T.W., Häusser M. Integration of quanta in cerebellar granule cells during sensory processing. Nature. 2004;428:856–860. doi: 10.1038/nature02442.
- Rancz E.A., Ishikawa T., Duguid I., Chadderton P., Mahon S., Häusser M. High-fidelity transmission of sensory information by single cerebellar mossy fibre boutons. Nature. 2007;450:1245–1248. doi: 10.1038/nature05995.
- Duguid I., Branco T., London M., Chadderton P., Häusser M. Tonic Inhibition Enhances Fidelity of Sensory Information Transmission in the Cerebellar Cortex. J. Neurosci. 2012;32:11132–11143. doi: 10.1523/JNEUROSCI.0460-12.2012.
- Ishikawa T., Shimuta M., Häusser M. Multimodal sensory integration in single cerebellar granule cells in vivo. Elife. 2015;4:e12916. doi: 10.7554/eLife.12916.
- Duguid I., Branco T., Chadderton P., Arlt C., Powell K., Häusser M. Control of cerebellar granule cell output by sensory-evoked Golgi cell inhibition. Proc. Natl. Acad. Sci. USA. 2015;112:13099–13104. doi: 10.1073/pnas.1510249112.
- Margrie T.W., Meyer A.H., Caputi A., Monyer H., Hasan M.T., Schaefer A.T., Denk W., Brecht M. Targeted Whole-Cell Recordings in the Mammalian Brain In Vivo. Neuron. 2003;39:911–918. doi: 10.1016/j.neuron.2003.08.012.
- Kitamura K., Judkewitz B., Kano M., Denk W., Häusser M. Targeted patch-clamp recordings and single-cell electroporation of unlabeled neurons in vivo. Nat. Methods. 2008;5:61–67. doi: 10.1038/nmeth1150.
- Jouhanneau J.-S., Ferrarese L., Estebanez L., Audette N.J., Brecht M., Barth A.L., Poulet J.F.A. Cortical fosGFP Expression Reveals Broad Receptive Field Excitatory Neurons Targeted by POm. Neuron. 2014;84:1065–1078. doi: 10.1016/j.neuron.2014.10.014.
- Jouhanneau J.-S., Kremkow J., Poulet J.F.A. Single synaptic inputs drive high-precision action potentials in parvalbumin expressing GABA-ergic cortical neurons in vivo. Nat. Commun. 2018;9:1540. doi: 10.1038/s41467-018-03995-2.
- Jouhanneau J.-S., Poulet J.F.A. Multiple Two-Photon Targeted Whole-Cell Patch-Clamp Recordings From Monosynaptically Connected Neurons in vivo. Front. Synaptic Neurosci. 2019;11:15. doi: 10.3389/fnsyn.2019.00015.
- Jouhanneau J.-S., Kremkow J., Dorrn A.L., Poulet J.F.A. In Vivo Monosynaptic Excitatory Transmission between Layer 2 Cortical Pyramidal Neurons. Cell Rep. 2015;13:2098–2106. doi: 10.1016/j.celrep.2015.11.011.
- Margrie T.W., Brecht M., Sakmann B. In vivo, low-resistance, whole-cell recordings from neurons in the anaesthetized and awake mammalian brain. Pflügers Arch. 2002;444:491–498. doi: 10.1007/s00424-002-0831-z.
- Poulet J.F.A., Fernandez L.M.J., Crochet S., Petersen C.C.H. Thalamic control of cortical states. Nat. Neurosci. 2012;15:370–372. doi: 10.1038/nn.3035.
- Yu J., Hu H., Agmon A., Svoboda K. Recruitment of GABAergic Interneurons in the Barrel Cortex during Active Tactile Behavior. Neuron. 2019;104:412–427.e4. doi: 10.1016/j.neuron.2019.07.027.
- Bitzenhofer S.H., Sieben K., Siebert K.D., Spehr M., Hanganu-Opatz I.L. Oscillatory Activity in Developing Prefrontal Networks Results from Theta-Gamma-Modulated Synaptic Inputs. Cell Rep. 2015;11:486–497. doi: 10.1016/j.celrep.2015.03.031.
- Guo Z.V., Inagaki H.K., Daie K., Druckmann S., Gerfen C.R., Svoboda K. Maintenance of persistent activity in a frontal thalamocortical loop. Nature. 2017;545:181–186. doi: 10.1038/nature22324.
- Inagaki H.K., Fontolan L., Romani S., Svoboda K. Discrete attractor dynamics underlies persistent activity in the frontal cortex. Nature. 2019;566:212–217. doi: 10.1038/s41586-019-0919-7.
- Lenschow C., Brecht M. Barrel Cortex Membrane Potential Dynamics in Social Touch. Neuron. 2015;85:718–725. doi: 10.1016/j.neuron.2014.12.059.
- Ebbesen C.L., Doron G., Lenschow C., Brecht M. Vibrissa motor cortex activity suppresses contralateral whisking behavior. Nat. Neurosci. 2017;20:82–89. doi: 10.1038/nn.4437.
- Clemens A.M., Lenschow C., Beed P., Li L., Sammons R., Naumann R.K., Wang H., Schmitz D., Brecht M. Estrus-Cycle Regulation of Cortical Inhibition. Curr. Biol. 2019;29:605–615.e6. doi: 10.1016/j.cub.2019.01.045.
- Harvey C.D., Collman F., Dombeck D.A., Tank D.W. Intracellular dynamics of hippocampal place cells during virtual navigation. Nature. 2009;461:941–946. doi: 10.1038/nature08499.
- Lee A.K., Manns I.D., Sakmann B., Brecht M. Whole-Cell Recordings in Freely Moving Rats. Neuron. 2006;51:399–407. doi: 10.1016/j.neuron.2006.07.004.
- Epsztein J., Lee A.K., Chorev E., Brecht M. Impact of Spikelets on Hippocampal CA1 Pyramidal Cell Activity During Spatial Exploration. Science. 2010;327:474–477. doi: 10.1126/science.1182773.
- Epsztein J., Brecht M., Lee A.K. Intracellular Determinants of Hippocampal CA1 Place and Silent Cell Activity in a Novel Environment. Neuron. 2011;70:109–120. doi: 10.1016/j.neuron.2011.03.006.
- Lee D., Lin B.-J., Lee A.K. Hippocampal Place Fields Emerge upon Single-Cell Manipulation of Excitability During Behavior. Science. 2012;337:849–853. doi: 10.1126/science.1221489.
- English D.F., Peyrache A., Stark E., Roux L., Vallentin D., Long M.A., Buzsáki G. Excitation and inhibition compete to control spiking during hippocampal ripples: Intracellular study in behaving mice. J. Neurosci. 2014;34:16509–16517. doi: 10.1523/JNEUROSCI.2600-14.2014.
- Böhm C., Peng Y., Maier N., Winterer J., Poulet J.F.A., Geiger J.R.P., Schmitz D. Functional Diversity of Subicular Principal Cells during Hippocampal Ripples. J. Neurosci. 2015;35:13608–13618. doi: 10.1523/JNEUROSCI.5034-14.2015.
- Hulse B.K., Moreaux L.C., Lubenov E.V., Siapas A.G. Membrane Potential Dynamics of CA1 Pyramidal Neurons during Hippocampal Ripples in Awake Mice. Neuron. 2016;89:800–813. doi: 10.1016/j.neuron.2016.01.014.
- Šišková Z., Justus D., Kaneko H., Friedrichs D., Henneberg N., Beutel T., Pitsch J., Schoch S., Becker A., von der Kammer H., et al. Dendritic Structural Degeneration Is Functionally Linked to Cellular Hyperexcitability in a Mouse Model of Alzheimer’s Disease. Neuron. 2014;84:1023–1033. doi: 10.1016/j.neuron.2014.10.024.